Эфиры
Содержание:
Показания и противопоказания
Показания для обеих форм препарата значительно отличаются друг от друга:
- В анестезиологии эфир для наркоза используется для разных способов ингаляционной подачи. Применяемые схемы:
- открытая, или капельная;
полуоткрытая;
полузакрытая;
закрытая.
Виды ингаляционного наркоза
Таблетированная форма Эфира, как уже отмечалось, используется в урологической и гинекологической практике. Назначение лекарства целесообразно при лечении:
пиелонефрита;
инфекционных патологий половых путей у женщин.
Таблетки Эфира назначаются также в профилактических целях пациентам, перенесшим хирургические вмешательства или операционные диагностические процедуры. Так, средство прописывается после цистоскопии, катетеризации, лапароскопических и лапаротомических вмешательств на мочевом пузыре или половых органах.

Побочные эффекты
Таблетированная форма Эфира не назначается:
- беременным женщинам;
- кормящим матерям;
- детям до 18 лет;
- пациентам с гиперчувствительностью к отдельным элементам, содержащимся в таблетках;
- больным с нарушением функционирования почек или печени;
- лицам с непереносимостью лактозы, дефицитом лактазы или глюкозо-галактозной мальабсорбцией.
Эфирный раствор имеет ряд других противопоказаний, которые должны учитываться врачом перед использованием средства для наркоза. Так, данная форма медпрепарата не может быть применена людям с:
- острыми или обострившимися хроническими заболеваниями органов дыхательной системы;
- повышенным внутричерепным давлением (ВЧД);
- патологиями сердечно-сосудистой системы, сопровождающимися значительным повышением АД, либо декомпенсированными нарушениями сердечной деятельности;
- тяжелым течением почечных и печеночных болезней;
- общим истощением организма;
- сахарным диабетом обоих типов;
- ацидозом.
Также ингаляционный Эфир не используется для анестезии пациентам, у которых повышенное возбуждение может вызвать серьезные нарушения в работе всего организма.
Производство
Ферментация
Этанол получают путем ферментации из биомассы, обычно из сахарных или крахмалосодержащих культур, или традиционно из садовых фруктов и овощей. Этот процесс осуществляется контролируемым образом с использованием ряда пищевых продуктов, например, вина из винограда или пива из солода и хмеля.
Крахмалосодержащее сырье (картофель и злаки) должно быть предварительно обработано для производства сбраживаемого сахара. Во время ферментации крахмал сначала расщепляется на дисахариды, гликозидные связи которых расщепляются гидролазами. Полученные моносахариды затем ферментируются дрожжами или бактериями. При концентрации этанола около 15% дрожжевые клетки и бактерии начинают умирать, что означает, что ферментация не может достичь более высокой концентрации. Общее уравнение алкогольного брожения:
Дистилляция
Питьевой спирт получают путем перегонки алкогольного сусла
из сельскохозяйственного сырья. В зависимости от процесса сгорания дистиллят
содержит ароматизаторы, сивушные масла и другие органические соединения,
которые определяют характер и вкус конечного продукта, такого как бренди, виски
или ром. Для производства водки используется почти чистый этанол, разбавленный
только водой. Чистый спирт используется неразбавленным в качестве исходного
материала для других алкогольных напитков, например, для большинства ликеров.
Алкогольные напитки, содержащие дистиллированный этанол,
называются спиртными напитками – в отличие от вина и пива, этанол которых
производится исключительно путем алкогольной ферментации.
Технический синтез
Этанол получают химическим синтезом из воды и этена в так называемом косвенном гомогенном каталитическом процессе с добавлением серной кислоты. Процесс проводится в две стадии с образованием сложных эфиров серной кислоты, которые должны быть гидролизованы на второй стадии. Серная кислота должна быть повторно сконцентрирована после гидролиза. В прямом процессе фосфорная кислота, нанесенная на кремнезем, действует как гетерогенный катализатор. Из-за проблем сточных вод и коррозии, вызванных использованием серной кислоты, в настоящее время этанол производится в промышленности путем катализа фосфорной кислоты. Общее уравнение для обоих процессов:
Строение этанола
В молекулах спиртов, помимо связей С–С и С–Н, присутствуют ковалентные полярные химические связи О–Н и С–О.
| Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4). |
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
Водородные связи и физические свойства спиртов
Спирты образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул спиртов:
Поэтому этанол – жидкость с относительно высокой температурой кипения (температура кипения этанола +78 о С).
Водородные связи образуются не только между молекулами спиртов, но и между молекулами спиртов и воды. Поэтому спирты очень хорошо растворимы в воде. Молекулы спиртов в воде гидратируются:
| Чем больше углеводородный радикал, тем меньше растворимость спирта в воде. Чем больше ОН-групп в спирте, тем больше растворимость в воде. |
Этанол смешивается с водой в любых соотношениях.
Фармакодинамика и фармакокинетика
Вещество вступает в не специфическое взаимодействие с мембранами нейронов головного, спинного и продолговатого мозга, в основном – с липидными двухслойными мембранами аксонов. Лекарство обратимо изменяет механизмы их работы и ультраструктуру. Средство сильно угнетает работу центральной нервной системы, блокирует процессы синаптического возбуждения. Сохраняя активность бульбарных центров, вещество функционально дезинтегрирует взаимодействия коры и подкорки гм. После воздействия лекарства на человека отмечаются традиционные стадии наркоза: обезболивание, возбуждение и трехуровневый хирургический наркоз. У пациента отсутствует сознание и все виды чувствительности, угнетаются рефлекторные реакции, и расслабляется скелетная мускулатура.
При проведении премедикации с помощью Диэтилового Эфира в сочетании с прочими общими анестетиками (ингаляционными и нет) значительно снижается функциональная активность нейронов коры гм. У пациента развивается амнезия, повышается активность подкорковых образований, проявляется психомоторное возбуждение, вариабельность пульса, ЧСС и АД. Также вещество раздражает слизистые оболочки, в том числе в ротовой полости, вызывает гиперсаливацию, рост бронхиальной секреции, ларингоспазм и кашель, расстройства дыхания и работы сердечно-сосудистой системы. Если слюна или слизь, насыщенная эфиром проникает в пищеварительный тракт, у пациента происходит рефлекторная стимуляция рвотного центра, тошнота вначале наркоза и после пробуждения.
При проведении хирургического наркоза наблюдается значительное угнетение межнейрональной передачи импульсов в спинном и головном мозге. Происходит рост активности отделов гипоталамуса, отвечающих за работу гипофиза, симпатической нервной системы и надпочечников, повышается секреция катехоламинов и глюкокортикоидов. Стимулируется выброс адреналина, наблюдается гипергликемия, рост АД, спазм сосудов внутренних органов, угнетается перистальтика кишечника. У пациента расслабляются скелетные мышцы, нарушается центральная регуляция мышечного тонуса.
При применении больших дозировок лекарственного средства наблюдается угнетение дыхания, работы сосудодвигательного центра, гипотензия. Вещество стимулирует охлаждение легочных тканей при скоплении в ней жидкости, что может привести к пневмонии. Нарушаются обменные процессы, работа печени и почек, снижается диурез, сужаются почечные сосуды.
Следует отметить, что эфирный наркоз легко контролировать. При вдыхании паров через маску эффект развивается достаточно медленно, в течение 15-20 минут. Пробуждение от наркоза происходит в течение 20-40 минут. Достаточно долго сохраняется сонливость, угнетение работы нервной системы и обезболивающий эффект. При сочетании вещества с миорелаксантами и барбитуратами у пациента не возникает неприятных ощущений удушья и страха, снижается риск возникновения депрессии после наркоза.
Диэтиловый Эфир легко преодолевает ГЭБ, быстро проникает сквозь межнейронную жидкость и распределяется по внутренним органам. Наибольшая концентрация достигается в головном, спинном и продолговатом мозге. На стадии анальгезии плазменная концентрация составляет до 25 мг, возбуждения – до 70 мг, и в стадии хирургического наркоза – до 110 мг.
Средство быстро преодолевает плацентарный барьер, задерживается в гепатоцитах. Около 15% принятой дозировки подвергается биотрансформации. В первые несколько минут вещество быстро выводится из организма, затем процесс замедляется, порядка 90% средства выделяется с дыханием, остальное – с помощью почечной секреции.
При применении медицинского эфира для аппликации на ткани зуба, он оказывает подсушивающий эффект. Обладает слабой антибактериальной и местной обезболивающей активностью. При наружном применении средство оказывает местно раздражающий и охлаждающий эффекты.
получение
Из этилового спирта
Этиловый эфир может быть получен из этилового спирта в присутствии серной кислоты в качестве катализатора. Серная кислота в водной среде диссоциирует с образованием иона гидроксония, H3О+.
Безводный этиловый спирт протекает через раствор серной кислоты, нагретый между 130 и 140 ° С, вызывая протонирование молекул этилового спирта. Впоследствии другая молекула непротонированного этилового спирта реагирует с протонированной молекулой.
Когда это происходит, нуклеофильная атака второй молекулы этилового спирта способствует выделению воды из первой молекулы (протонированной); в результате образуется протонированный этиловый эфир (СН3СН2OHCH2СН3), с частично заряженным положительным кислородом.
Однако этот метод синтеза теряет эффективность, поскольку серная кислота разбавляется водой, образующейся в процессе (продукт дегидратации этилового спирта).
Температура реакции является критической. При температуре ниже 130 ° C реакция протекает медленно и по большей части этиловый спирт будет перегоняться.
При температуре выше 150 ° C серная кислота вызывает образование этилена (алкена с двойной связью) вместо объединения с этиловым спиртом с образованием этилового эфира.
Из этилена
В противоположном процессе, то есть при гидратации этилена в паровой фазе, этиловый эфир может образовываться в качестве побочного продукта в дополнение к этиловому спирту. На самом деле, этот синтетический путь производит большую часть этого органического соединения.
В этом процессе используются фосфорно-кислотные катализаторы, закрепленные на твердой подложке, которые можно регулировать для получения большего количества эфира.
Обезвоживание в паровой фазе этанола в присутствии глиноземных катализаторов может дать 95% выход при производстве этилового эфира.
История
Возможно, что впервые диэтиловый эфир был получен в IX веке алхимиком Джабир ибн Хайяном либо алхимиком Раймундом Луллием в 1275 году. Достоверно известно, что он был синтезирован в 1540 году Валерием Кордусом, который назвал его «сладким купоросным маслом» (лат. oleum dulce vitrioli), поскольку получил его перегонкой смеси этилового спирта и серной кислоты, которая тогда называлась «купоросным маслом». Кордус также отметил его анестезирующие свойства. В 1680 году Роберт Бойль вторично синтезировал эфир. Затем в 1704 году Исаак Ньютон открыл эфир в третий раз, в поисках синтеза искусственного золота.
Название «эфир» было дано этому веществу в 1729 году Фробениусом.
В 1794 году эфир был испытан для вдыханий с целью уменьшения болей, а в 1795 году Томас Беддоус создал Медицинский пневматический институт для лечения различных легочных заболеваний газами. Такие газы тогда называли «искусственным воздухом».
Как из этанола получить диэтиловый эфир
Методы получения эфира. Этиловый эфир можно получать различными способами. Однако вследствие своей простоты и дешевизны преимущественное распространение получили способы, основанные на отнятии какими-либо водоотнимающими средствами (концентрированными серной и фосфорной кислотами, ароматическими сульфокислотами, а также некоторыми безводными солями) молекулы воды от двух молекул спирта по схеме: 2С2Н5ОН С2Н5ОС2Н5 + Н2О Сернокислотный метод. Как показали исследования Вильямсона (1851-1852 гг.), реакция образования эфира из спирта при помощи серной кислоты протекает в две фазы. Сначала образуется сложный эфир спирта и серной кислоты: ОН СН3СН2ОН + SО2 Н2О + СН3СН2ОSО2 ОН, ОН называемый этилсерной кислотой. Этот продукт устойчив при умеренных температурах. Дальнейший нагрев этилсерной кислоты до 140°С с избытком спирта ведет к ее разложению на серную кислоту и диэтиловый эфир: ОН СН3СН2ОSО2 ОН + СН3СН2ОН SО2 + СН3СН2ОСН3СН2 ОН Если процесс проводить с самого начала при 140°С и вводить спирт в систему постепенно, то эфир отгоняется непрерывно, и теоретически процесс может продолжаться бесконечно. Однако в действительности кислота разбавляется водой и частично восстанавливается до сернистой кислоты, что обусловливает, в конечном итоге, прекращение процесса эфирообразования (эфиризации). Сандерен нашел, что прибавление к реагирующей смеси сернокислого алюминия или свинца в количестве 5% от веса смеси значительно облегчает образование эфира, которое в этом случае происходит уже при 120°С. Сернокислый алюминий действует при этом как катализатор, образуя промежуточную двойную соль этилсерной кислоты (SO4)2Al2SO4HC2H5. Также действует сернокислый свинец. Ведение процесса эфирообразования при избытке приливаемого к серной кислоте спирта обусловливает большую производительность и получение более чистого продукта. При нагреве этилсерной кислоты выше 200°С происходит почти количественная её диссоциация по уравнению: СН3СН2ОSО2 ОН СН2=СН2 + Н2SО4. Если эфирообразование ведется без избытка спирта, некоторый распад этилсерной кислоты происходит и при более низких температурах (125-140°С). При дегидратации, параллельно с образованием эфира, происходит частичное окисление спирта до ацетальдегида. Последний легко окисляется в уксусную кислоту: СН3СНО + О2 2СН3СООН, которая повышает кислотность образовавшегося продукта. При применении серной кислоты, содержащей соли железа, реакция окисления спирта идет более интенсивно. При получении эфира, особенно из спирта-сырца, помимо альдегида образуется также и ряд других побочных продуктов, раскисляющих серную кислоту. Из них в первую очередь надо отметить: продукты осмоления уксусного альдегида, этилен, сернистый газ, сульфоновые кислоты и так называемое «винное масло». Последнее состоит из простых и сложных эфиров, кетонов и углеводородов. Удельный вес масла равен 0,9; оно кипит в пределах 150-200°С. Основная часть «винного масла» кипит при 150-170°С и содержит этиламиловый эфир, этиламиловый кетон и диэтилсульфаты. Несмотря на загрязнение серной кислоты в процессе производства эфира, срок службы её довольно значителен. Реакция образования эфира из этилового спирта экзотермична. Количество выделяющегося при 125°С тепла, найденное расчетным путем, равно 8,59 ккал/гмоль или 8590_74=116 ккал/кг. Теплота сгорания эфира при 15°С – 8910 ккал/кг. ООО «Кузбассоргхим» производит эфир медицинский (ФСП 42-0473-4635-03) сернокислотным методом по реакции этерификации с последующей очисткой химическими растворами в соответствии с разработанным и утвержденным в установленном порядке промышленным регламентом на производство эфира медицинского ПР 43852015-02-2002. Существующий технологический процесс разработан НИИХП г. Казань для ПО «Прогресс» (п/я Р 6718, объект 430/416), входившего в состав оборонного комплекса, преемником которого в кадровой, технической и технологической политике с 1996 года является ООО «Кузбассоргхим». Год ввода в эксплуатацию производства эфира медицинского 1976, мощность производства 1350 тонн. Способ производства эфира медицинского ООО «Кузбассоргхим» за это время был оптимизирован в части усовершенствования способов очистки, но значительных изменений в технологии изготовления эфира диэтилового не произошло.
При регистрации сайта Вы получаете пароль для управления сайтом, который подходит для входа в личный кабинет — зарегистрироваться
Вход в личный кабинет
Визитов экспресс-сайтов сегодня: 4994
http://ximicat.com/info.php?id=192http://www.chem21.info/info/686180/http://www.himsite.ru/annonce/153
Этиловый эфир
Этиловый эфир выпускают согласно ГОСТ 6265 — 52 следующих марок: технический, медицинский и медицинский для наркоза.
Этиловые эфиры образуются количественно по отношению к кислотам. Они представляют собой бесцветную, прозрачную жидкость со специфическим запахом, характерным для легких эфиров. Температура выкипания-120 — 180 С, удельный вес при 20 С-082. Эти эфиры хорошо растворяют нитроцеллюлозу, глифтале-вые, поливинилхлоридные и алкидные смолы.
Этиловый эфир обладает низкой температурой самовоспламенения ( 180 — 200 С при атмосферном давлении), высоким давлением насыщенных паров и широкими пределами воспламеняемости. Снижение температуры сжатия от 300 до 190 — 220 СС при впрыске этилового эфира позволяет запустить двигатель при температуре примерно на 50 С ниже, чем на топливе. Однако при введении чистого эфира наблюдается высокая скорость нарастания давления в цилиндре двигателя, что может привести к поломкам деталей двигателя. Поэтому для смягчения жесткости работы двигателя в состав пусковых жидкостей, помимо масла, согласно патентным описям вводятся такие компоненты, как альдегиды, более высококипящие эфи-ры, амины, нитриты, нитраты, а также парафиновые углеводороды, преимущественно низкокипящие, и другие соединения. В результате этого содержание этилового эфира в пусковых жидкостях, как правило, не превышает 60 — 70 % и поэтому эффективность их несколько снижается.
Этиловый эфир пировипоградпой кислоты ( СНзССОС Н5) образует кеталь легче, чем ацетон.
Этиловый эфир — бесцветная, весьма подвижная и летучая жидкость со своеобразным приятным запахом. Смешивается с этанолом, бензолом, хлороформом и многими другими органическими растворителями. Растворимость в 100 мл воды — 7 5 г. С водой образует постоянно кипящую смесь при 34 15 С, содержащую 1 3 % воды.
Этиловый эфир 1-цианкоричнои кислоты О, О-Дибутилбутадиен — 1 3-фосфонат О.
Этиловый эфир 1-циан — 2-винилциклопропан — 1-кар-боновой кислоты, этиловый эфир 2-имино — З — циан-4 — винилциклопентан-1 — карбоновой кислоты и этиловый эфир 2-имино — 3-циан — 5-винилцикло-пентан — 1-карбоновой кислоты С.
Этиловый эфир ( C2Hs) 2O называется иногда обыкновенным, или серным, эфиром.
Этиловый эфир находит разностороннее применение, особенно в качестве хорошего растворителя. В медицине его употребляют для наркоза и усиления сердечной деятельности.
Этиловый эфир применяется для наркоза.
Этиловый эфир n — аминобензойной кислоты применяется в качестве анестезирующего средства под названием анестезина.
Этиловый эфир является важнейшим растворителем в практике лабораторного органического синтеза и в производствах тонких органических продуктов. Его применяют также в больших количествах в смеси с этиловым спиртом для растворения нитроцеллюлозы и в производствах бездымного пороха, коллодия и кинопленки. Имеет широкое применение и в медицине.
Этиловый эфир е / порично-бутилмалоновой кислоты удобно получать из бромистого шорично-бутила и малонового эфира по общему способу, описанному в Синт. Указанный выше выход р-метилвалериановой кислоты был получен при применении полученного данным способом этилового эфира ето / шчно-бутилмалоновой кислоты.
Этиловый эфир применять нельзя, так как его температура кипения близка к температуре кипения пентана.
Этиловый эфир р-фенил fi — оксипропионовой кислоты , В чистую сухую пол-литровую грехгорлую — колбу, сяаб жснную механической мешалкой, делительной воронт кой на 250 мл и обратным холодильником с хлоркальцне-вой трубкой, помещают 40 г ( 0 62 моля) очищенной цинковой пыли или гранулированного цинка, В делительную воронку наливают раствор 83 5 г ( 0 50 моля) бромуксусно-го эфира и 65 г ( 0 61 моля) бензальдегида в 80 мл сухого бензола и 20 мл абсолютного эфира.
История эфира
Диэтиловый эфир, который используется для современного наркоза, был впервые получен алхимиками в 9 веке. Чуть больше информации о нем появляется только к середине 16 века, когда это вещество получают путем перегонки этилового спирта и серной кислоты. В то же время отмечаются анестезирующие свойства эфира. Свое название соединение получает в 1729 году (от др.греч. aetherus – «верхний слой воздуха»).
Широкое применение в анестезиологии диэтиловый эфир находит в начале 19 века, когда его используют для вдыхания с целью снижения болевой чувствительности. С этого времени начинается активное развитие химии, и поисками средств для обезболивания во время операций интересуются ученые и доктора разных стран.
Знаменитый отечественный хирург Н.И.Пирогов тоже использовал диэтиловый эфир для наркоза при проведении полевых операций во время Крымской (1853-1856) и Русско-турецкой (1877-1878) войн. Тогда еще сложно было контролировать количество подаваемого больному газа, и некоторые солдаты умирали от передозировки. Но спасено было гораздо больше жизней, т.к. врач получал возможность спокойно оперировать глубоко «уснувших» пациентов, не испытывающих болевого шока.
Влияние на здоровье
Этанол всасывается по всему пищеварительному тракту. Первый
этап в небольшой степени начинается уже в слизистой оболочке полости рта.
Поглощенный там спирт поступает непосредственно в кровь и, таким образом,
распределяется по всему телу, включая мозг. Около 20% всасывается в желудке,
остальное в тонкой кишке.
Этанол, абсорбированный в желудке и кишечнике, сначала
попадает в печень вместе с кровью, где он частично разлагается. Всасывание
спирта увеличивается за счет различных факторов, таких как тепло (ирландский
кофе, грог), сахар (ликер) и углекислый газ (игристое вино).
Приблизительно 2-10% выпитого спирта выделяется с мочой,
потом и выдыхаемым воздухом.
В печени, основная часть этанола (как и другие растворимые в
воде токсины) с помощью ферментов алкогольдегидрогеназы (АДГ) деградируют спирт
до уксусной кислоты. Уксусная кислота затем превращается в CO2 через цикл
Кребса. Промежуточный этанал отвечает за так называемые симптомы «похмелья» –
головная боль, тошнота и рвота. Разложение этана сдерживается сахаром, поэтому
похмелье бывает особенно интенсивно при употреблении сладких алкогольных напитков,
особенно ликера и некоторых сортов шампанского.
Скорость деградации алкогольдегидрогеназой является
постоянной в определенных пределах. У мужчин это около 0,1 г в час и кг массы
тела, у женщин 0,085
Токсикология
Этанол не классифицируется ни как яд, ни как вредный для
здоровья элемент. Но патологи считают его «гепатотоксическим веществом», то
есть прямым токсином печени. А педиатры называют его «тератогенным ядом»,
который может поврежить плод.
Излишнее потребление спирта приводит к типичным симптомам острой интоксикации, таким как головокружение, тошнота, дезориентация, разговорчивость и повышенная агрессия. Летальная доза (ЛД) составляет приблизительно от 3,5 до 4,0 промилле.
Другие статьи
Применение
Ингаляционная общая анестезия по открытой (капельно), полуоткрытой, полузакрытой и закрытой системам (в основном при кратковременных хирургических вмешательствах).
Поддержание общей анестезии при проведении комбинированной общей анестезии с применением психоактивных ЛС и периферических миорелаксантов.
Гиперчувствительность, острые заболевания дыхательных путей, внутричерепная гипертензия, артериальная гипертензия; ХСН, печеночная и/или почечная недостаточность, кахексия, сахарный диабет, ацидоз.
Необходимость проведения в ходе хирургического вмешательства электрокоагуляции или использования электроножа.
Кашель, психомоторное возбуждение, повышение АД, тахикардия, гиперсекреция бронхиальных желез; тошнота и рвота.
В послеоперационном периоде — рвота, угнетение дыхательного центра; бронхопневмония, бронхит, ларингит, трахеит, отек легких (токсического генеза), парез кишечника, снижение секреции желчи, метаболический ацидоз, снижение клубочковой фильтрации и диуреза.
Получение эфира из спирта
Получение диэтилового эфира интересно тем, что очень убедительно показывает учащимся влияние условий реакции на образование разных продуктов из одних и тех же исходных веществ. Этиловый спирт и концентрированная серная кислота при нагревании выше 140- 150°С дают преимущественно этилен (с. 46), при температуре ниже 140°С дают диэтиловый эфир.
На результат реакции оказывают влияние и относительные количества взятых веществ. При получении эфира относительное количество спирта должно быть больше, чем при получении этилена. Это объясняется тем, что эфир образуется при действии на этилсерную кислоту дополнительного количества спирта:
тогда как этилен получается при разложении этилсерной кислоты:
Учащимся это может быть разъяснено так: при образовании молекулы этилена серная кислота отнимает воду от каждой молекулы спирта, а при образовании эфира она отнимает воду от каждых двух молекул спирта:
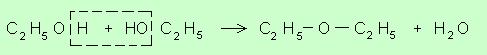
Опыт ведут так, чтобы вначале получить этилсерную кислоту, а затем к ней добавляют спирт и отгоняют эфир, нагревая жидкость не выше 140°С.
В небольшую колбу
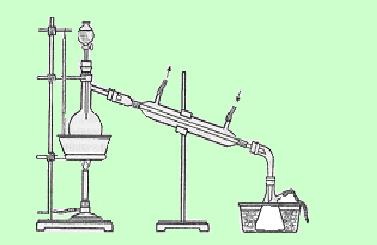
наливают равные по объему количества спирта (ректификата) и концентрированной серной кислоты, что соответствует примерно эквимолекулярным соотношениям. В воронку наливают дополнительное количество спирта. В качестве приемника используют колбу Бунзена, которую ставят в сосуд со льдом и к боковой трубке его присоединяют длинную каучуковую трубку для отвода несконденсировавшихся паров эфира (под тягу или за окно).
Нагревают колбу на песчаной бане (песок должен быть нагрет заранее) до температуры 140°С и, когда начнет перегоняться эфир, добавляют понемногу из воронки этанол. Через холодильник должна идти сильная струя холодной воды. Опыт ведут до получения необходимого для демонстрации количества эфира. С эфиром неизбежно отгоняется некоторое количество спирта и воды. Чтобы эфир отмыть от спирта, дистиллят переносят в делительную воронку, добавляют к нему равный объем воды, содержимое воронки взбалтывают, дают жидкости отстояться, сливают нижний водный слой, а эфир переносят в пробирку и демонстрируют классу.
После удаления спирта эфир промывают слабым раствором щелочи, освобождаясь от кислот, затем снова промывают водой и сушат хлоридом кальция. Эти операции выполняют уже не на уроке.
Отсутствие донорных атомов водородной связи
Если вы внимательно посмотрите на структуру, вы заметите отсутствие атома, способного отдавать водородную связь. Однако такими акцепторами являются атомы кислорода, и благодаря этилацетату он хорошо растворяется в воде и в значительной степени взаимодействует с полярными соединениями и донорами водородных связей (такими как сахара).
Кроме того, это позволяет ему превосходно взаимодействовать с этанолом; причина, по которой его присутствие в алкогольных напитках неудивительно.
С другой стороны, его алкоксигруппа позволяет ему взаимодействовать с некоторыми неполярными соединениями, такими как хлороформ, CH 3 Cl.
Аналоги
Медицинский Эфир для анестезии очень трудно найти в аптеках в чистом виде, поэтому пациент и его лечащий врач должны заблаговременно обсудить лекарства, которыми можно заменить рассматриваемое средство. Сразу отметим, что абсолютных аналогов эфирного наркоза не существует, но при необходимости вместо него могут быть использованы следующие средства для ингаляционного наркоза:
-
Севоран. Действующее вещество – севофлуран. Лекарство оказывает быстрое воздействие. После начала ингаляционной подачи анестетика отключение сознания происходит за считанные минуты. Привести пациента в чувство можно только после полного прекращения распыления Севорана.
- Закись азота. Средство для общего наркоза, используемое преимущественно в комбинации с кислородом посредством ингаляционной подачи. Препарат оказывает слабое наркотическое действие, поэтому для усыпления пациента его приходится применять в высоких дозировках. Отпускается по рецепту.
- Трихлорэтилен. Этот медикаментозный препарат отличается довольно сильным наркотическим воздействием. Применяется, как правило, для кратковременного отключения сознания у пациентов при необходимости относительно простых хирургических вмешательств.
- Фторотан. Еще одно сильнодействующее средство, предназначенное для ингаляционного наркоза. Раствор быстро действует и так же быстро выводится из организма. Лекарство для анестезии может быть применено как самостоятельно, так и в комплексе с закисью азота.
Все вышеперечисленные препараты отпускаются из аптек исключительно по рецепту. Они непригодны для самолечения, поскольку способны вызывать серьезные и даже опасные побочные действия.






